生物制药工艺强化(Process Intensification, PI)已从概念探索阶段迈入工业化实施的关键时期,其终极目标被广泛认同为:建立一个高度整合、无缝衔接的端到端(End-to-End)连续流工艺。这一目标代表着对传统批次生产模式的根本性颠覆,旨在解锁生物制药制造的效率、灵活性与质量潜能。
传统批次工艺的局限性
传统批次工艺的核心痛点在于其固有的“离散”特性。上游的批次/补料批次培养与下游的间歇纯化单元之间存在着物理和时间上的割裂。
规模放大悖论: 为追求高产量而扩大设备规模(如反应器体积、层析柱尺寸),显著增加资本支出和运营成本,同时复杂化了工艺验证与厂房设施要求。
动态不一致性: 各单元操作在时间、空间上的分离,使中间产物经历了非受控的滞留与条件波动(如产物降解、聚集风险增加),威胁最终产品质量属性的批内与批间一致性。
资源利用低效: 设备在批次切换、清洗、灭菌及等待过程中大量闲置,整体设备利用率低下,产能弹性受限。
连续流工艺通过将生产流程组织成一系列相互连接、持续运行的单元操作,使物料(细胞、产物、缓冲液)连续、持续通过整个系统(从种子扩增到最终制剂),从而在根本上解决上述痛点。
端到端连续流工艺:整合的力量
端到端连续流工艺的核心在于以“连续”和“整合”为原则。
连续上游生产
高密度灌流培养:采用灌流培养技术,细胞在生物反应器中长期维持高密度、高活率状态。新鲜培养基持续流入,同时含目标产物和代谢废物的培养液持续流出,进入下游处理。这消除了批次培养的终点限制,显著提升单位时间、单位体积的产物生产率(g/L/day),并允许使用更小体积的反应器。
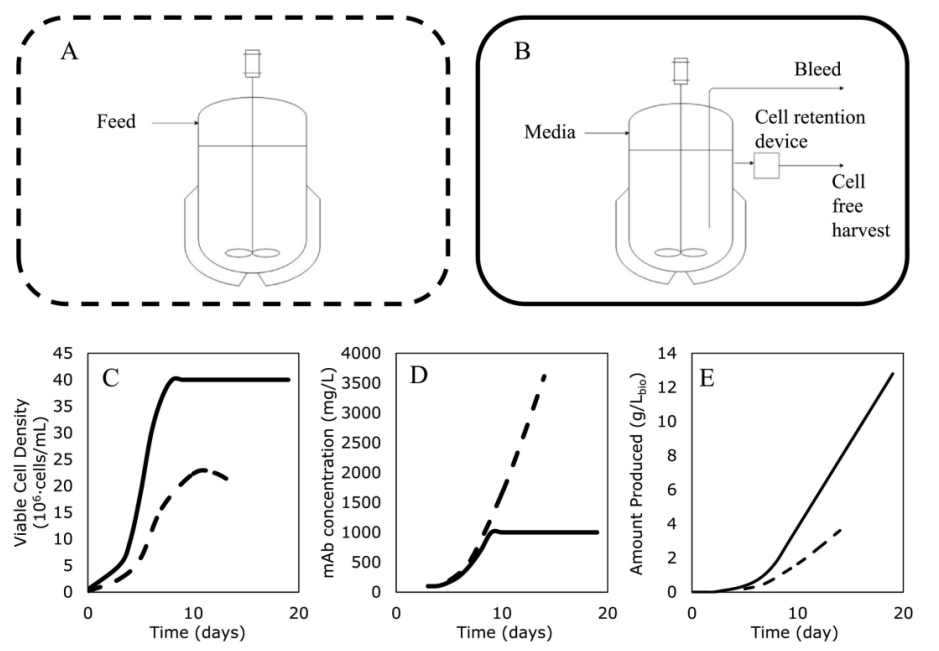
生产 mAb 的细胞系的补料分批 (A) 和灌注 (B) 过程示意图。细胞密度 (C)、生物反应器内的蛋白质浓度(D) 和总生产率 (E);虚线代表补料分批,实线代表灌注。[1]
种子扩增工艺: 结合一次性生物反应器和基于灌注的N-1种子扩增策略,实现快速、稳健的种子供应,与生产反应器高效衔接。
连续下游纯化
连续捕获: 利用多柱层析技术(如模拟移动床SMB、周期性逆流层析PCC)或连续流沉淀/过滤,持续处理上游灌流收获液。层析树脂载量利用率大幅提升,缓冲液消耗显著降低,设备尺寸显著缩小。
连续精纯与制剂: 整合连续流超滤/透析(TFF)、多柱层析精纯步骤以及在线稀释、混合、灌装技术。这不仅缩小设备规模,更关键的是减少了中间产物的暂存时间,最大限度降低降解风险,保障产品关键质量属性(CQAs)的稳定性。
过程分析技术 (PAT)与自动化控制
整个连续流程高度依赖于实时在线的传感器(如pH、DO、代谢物、产物浓度、杂质监测)和先进过程控制(APC)策略。PAT提供对关键工艺参数(CPPs)和质量属性的即时反馈,自动化控制系统则确保整个流程稳态运行、快速响应扰动并实现闭环控制,这是维持工艺稳健性的基石。
整合平台与数字化管理
物理单元通过无缝连接的流路(含在线混合、调节、取样点)整合。同时,数字化平台(如MES、LIMS)实现从上游灌流到最终制剂的全流程数据采集、监控、分析和追溯,为质量源于设计(Quality by Design, QbD)和实时放行检测(RTRT)提供强大支持。
关键挑战与应对策略
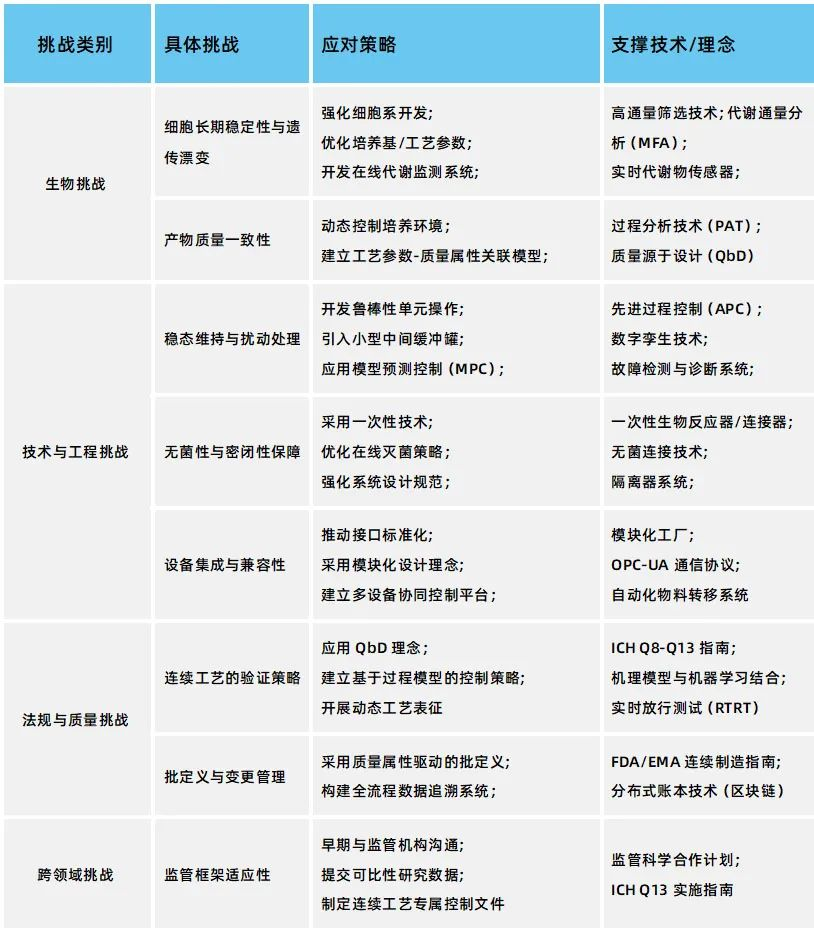
端到端连续流生物工艺的核心战略价值在于通过全流程的整合与连续化运作,实现显著的设备与设施小型化、产品质量与一致性提升、生产灵活性与供应链韧性增强,以及资源利用效率与可持续性优化。

Akwa® PAT在线过程分析系统
Akwa® PAT是由浚真生命科学自主研发的用于关键工艺参数(CPP)和关键质量参数(CQA)持续监测和优化的在线过程分析系统。包括Akwa®Cyte在线细胞传感器 、Akwa®Raman在线拉曼分析仪和Akwa®UV在线纯化和分离过程分析系统,助力生物药企通过先进的PAT技术确保产品质量及一致性,从而减少浪费、降本增效、实现高效工艺和技术转移。

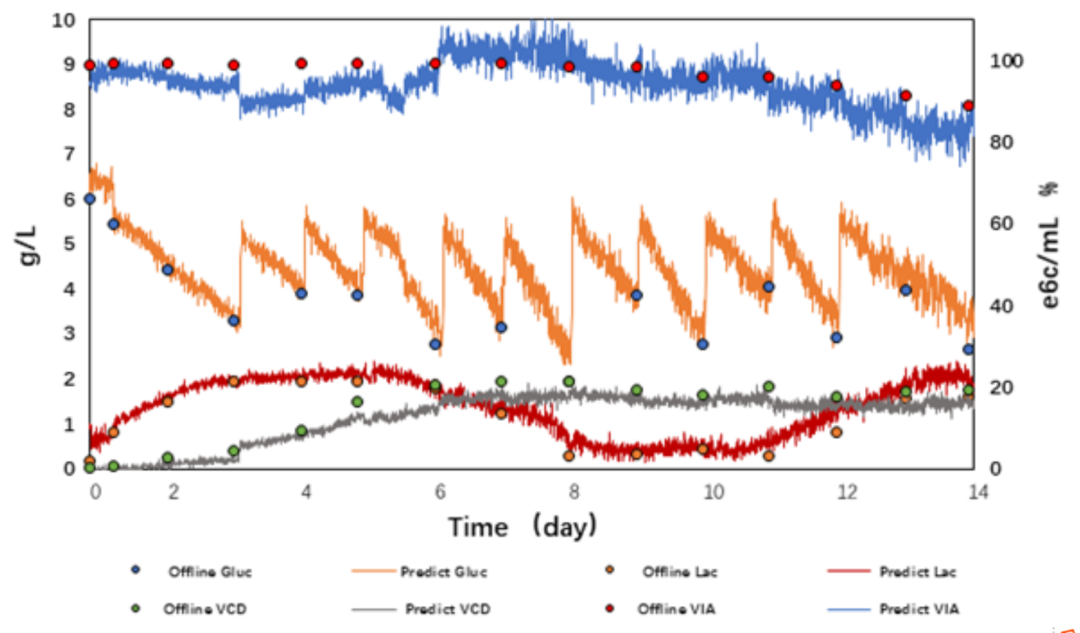
端到端连续流工艺从根本上保障了药品供应的安全性和韧性,推动生物制药工艺向“数智4.0”转型升级,驱动行业其向着更高效、灵活、敏捷、高质量和可持续的未来坚定迈进。这场革命终将加速创新生物药的开发与可及,惠及全球患者。
参考资料:
[1]Bielser, J.-M., Wolf, M., Souquet, J., Broly, H., & Morbidelli, M. (2018). Perfusion mammalian cell culture for recombinant protein manufacturing – A critical review. Biotechnology Advances, *36*(4), 1328–1340.