细胞计数仪是生物制药领域中不可或缺的工具,广泛应用于细胞培养、药物开发、疫苗生产和质量控制等多个环节。随着生物制药行业的快速发展,对细胞计数仪的合规性要求也日益严格。合规性不仅关系到产品的质量和安全性,还直接影响到药品的有效性和市场准入。
合规性是指企业在运营过程中,必须遵守相关的法律法规、行业标准和内部规章制度,以确保所有活动的合法性和规范性。在生物制药行业,细胞计数仪的合规性主要体现在以下几个方面:
数据完整性
根据FDA 21 CFR Part 11和《中国药品生产质量管理规范》等法规的要求,细胞计数仪必须确保数据的完整性、一致性和准确性。这包括数据的可追溯性、易读性、同时性、原始性和准确性,即ALCOA原则。近年来,FDA对数据完整性做了补充,增加了CCEA原则,即完整性、一致性、持久性和可取性,统称ALCOA+。
用户权限和审计追踪
细胞计数仪的软件系统应设置不同层级的用户权限,确保每个用户都有唯一的账号和密码,并且所有操作都有清晰的电子记录,以便进行审计追踪。这有助于企业实现数据的可追溯性和安全性。
系统和数据的安全性
细胞计数仪的操作系统和分析软件应具备高度的安全性,能够防止恶意软件的入侵和数据的非法篡改。同时,数据应保存在安全的数据库中,以确保其不易被删除或篡改。
保障产品安全性
合规性确保细胞计数仪在使用过程中的安全,降低因设备故障导致的药品质量问题。
提升数据可靠性
合规的设备经过严格验证,能够提供准确的细胞计数结果,确保药品研发和生产过程中的数据可靠性。
满足监管要求
生物制药行业受到严格监管,合规性是产品获得市场准入的基本条件。
CytScop®Pro是浚真生命科学自主研发的全自动、高通量、双荧光智能细胞计数仪,用于监控生物制药企业培养流程细胞计数和活力分析。

该设备在设计上充分考虑了合规性和数据完整性的要求,其内置软件符合中国国家药品监督管理局《药品生产质量管理规范(GMP)》以及美国食品药品监督管理局(FDA)有关电子记录和电子签名的规则(符合21 CFR Part 11要求),并遵循数据完整性指南(ALCOA+)原则。这意味着该设备在生成和分析数据时,能够确保数据的真实性、完整性和可追溯性,满足生物制药行业对合规性的严格要求。
启用软件中的安全选项,系统会自动授权用户调节以下配置,以实现合规。


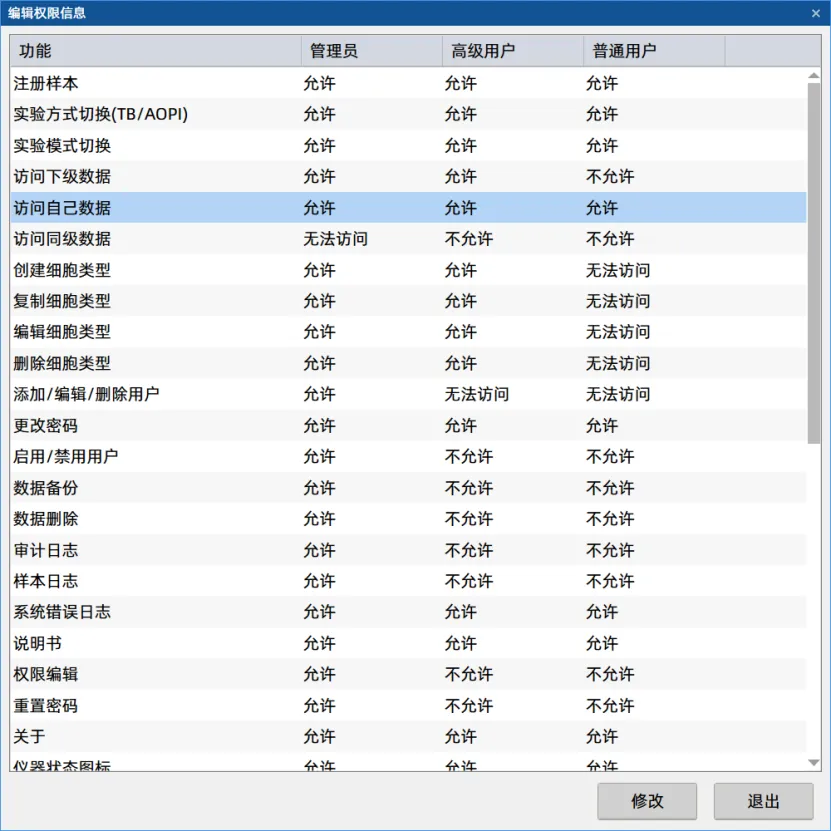
审计日志统计
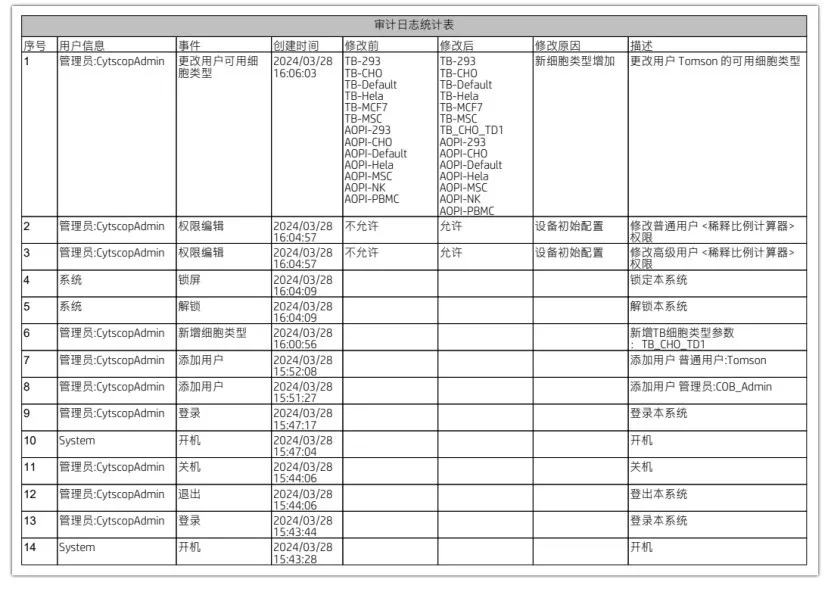
从法规标准到质量管理体系,从验证确认到持续监控,合规性贯穿于细胞计数仪的整个生命周期。随着生物制药行业的发展,CytScop Pro细胞计数仪的合规性管理也与时俱进,以确保其在药品研发和生产中的有效性和可靠性。通过全面的合规性管理,能够更好地服务于生物制药行业,为人类健康做出更大的贡献。